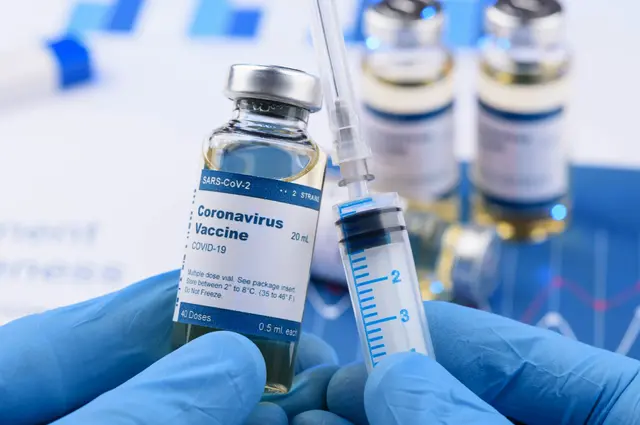
13日,美國疾控中心(CDC)主任雷德菲爾德發表聲明稱,已經正式簽署了輝瑞新冠疫苗的許可,允許在美國推進疫苗接種工作,疫苗的配送任務隨之開啓。消息人士還透露,14日起,將向包括美國總統特朗普在內的高級官員提供疫苗。
全美疫苗配送任務展開預計2021年3月底前爲1億人接種
當地時間11日晚,美國食品和藥物管理局(FDA)給予美國輝瑞與德國生物新技術公司聯合研發的新冠疫苗以緊急使用授權。這是首款獲批在美緊急使用的新冠疫苗。一天後,CDC的顧問小組也投票建議16歲及以上的人羣使用該疫苗。
13日,雷德菲爾德表示已正式簽署疫苗許可後,當日凌晨,輝瑞公司的第一批新冠疫苗從該公司位於密歇根Portage的工廠起運。大約184275小瓶疫苗被裝載在大約190個盒子中,然後裝上貨車,該款疫苗的全美配送正式開始展開。
美國政府新冠疫苗研發計劃“神速任務”(Operation Warp Speed)首席顧問斯勞伊13日稱,美國預計要在2021年3月底之前爲1億人接種疫苗。他還指出,美國希望在12月底之前配送大約4000萬劑疫苗。其中還包括莫德納(Moderna)的疫苗。
據報道,美國另一藥廠莫德納的新冠疫苗將在17日由FDA專家組進行討論,有望成爲第二種在美國批准使用的新冠疫苗。
特朗普等官員今起可接種
據報道,美國首輪的新冠疫苗接種計劃最早將從當地時間14日開始,但大部分民衆預計要在2021年春夏才能注射。而誰能優先注射疫苗,則由聯邦政府授權各州自行決定,這引發安排方面的憂慮。
CDC日前建議,應考慮將風險較高的醫護、養老院的長期居住者及護理人員作爲新冠疫苗的首批接種對象。但肯塔基、密西西比、紐約等州直接將疫苗分配權下放給醫院,理由是相信醫院有能力分辨哪些人應該接種疫苗。
部分人士指此舉合理,因爲首批疫苗量少且時間匆促。但也有批評者認爲,交給醫院自行處理將打亂州層次上的統一安排,破壞疫苗分配透明公平原則。約翰斯·霍普金斯大學健康安全研究中心研究員託納指,“無論是現狀抑或是未來安排,都可能一團亂。”
另一方面,有知情人士13日透露,將從14日開始,向美國總統特朗普和副總統彭斯,以及其他美國高級官員提供批准的輝瑞新冠疫苗。白宮的必要員工和聯邦政府三個分支部門的特定官員將在未來10天內接種疫苗。
4人接種疫苗出現面癱僅一半美民衆願意接種疫苗
FDA近日發表的一份報告中指出,在這款新冠疫苗的臨牀試驗中,有4名志願者出現面部癱瘓症狀,當局估計是因病毒感染導致面部神經發炎。
FDA表示,4人出現症狀的時間介於3天到48天之間,皆在3周內恢復正常,顯示症狀只是暫時性的,並“剛好”且“隨機”出現在疫苗組的。相關人員指出,症狀發生的確切原因還有待調查,現階段無法確認是否與疫苗有關。
FDA此前表示,絕大部分美國人都可以注射該款疫苗,僅擁有嚴重過敏史的人羣不建議注射,該人羣預計只佔人口的1.6%。
雖然,FDA認可的臨牀試驗數據顯示,該疫苗在預防新冠病毒感染方面有95%的有效率。但一項民調顯示,在各州準備開始第一輪新冠疫苗注射時,只有大約一半的美國民衆想接種疫苗,而四分之一的人不確定他們會接種,還有四分之一的人明確表示他們不會接種。
斯勞伊說,公衆對疫苗功效或安全性的懷疑“並沒有基於任何事實或數據”,並強調快速批准疫苗的程序中不存在偷工減料。
(來源:中新網)
 简体中文
简体中文